Líquidos iónicos, ¿Solventes del futuro?.
Una sustancia química que puede dar solución a todos estos problemas son los líquidos iónicos. Para comprender estos a continuación estudiaremos y analizaremos la naturaleza de este tipo de sustancias y las características que las hacen tan especiales.
Líquidos Iónicos.
Los líquidos iónicos (LIs) han sido aceptados como una nueva revolución de la química verde la cual influye tanto académicamente como en la industria química. Este nuevo grupo químico puede reducir el uso de solventes orgánicos peligrosos y contaminantes debido a sus características únicas. Los términos líquido iónico a temperatura ambiente (LITA), líquidos iónicos no acuosos, sales fundidas y sal orgánica liquida han sido usados para describir estos tipos sales en fase liquidas. Los líquidos iónicos están compuestos completamente por iones, son conocidos como sales que son liquidas a temperatura ambiente en contraste a las sales fundidas a altas temperaturas. Los líquidos iónicos tienen un conjunto de propiedades físico-química únicas las cuales les permiten ser empleado en numerosas aplicaciones en las cuales los solventes orgánicos convencionales no son lo suficientemente efectivos o no aplicables. En comparación al año 1980, donde solo existía un poco de patentes registradas para la aplicación de los LIs, en el año 2000, el número de patentes para la aplicación incremento a 100, y para finales del 2004, existían más de 800 patentes. Esto es claramente un indicador de la alta afinidad de la academia y la industria hacia los líquidos iónicos.
 Figura 1. Líquidos Iónicos.
Figura 1. Líquidos Iónicos.Características de los Líquidos Iónicos.
Los líquidos iónicos están formados de iones cargados positiva y negativamente, mientras que el agua y solventes orgánicos, como el tolueno y el diclorometano, están formados de moléculas. La estructura de los LIs es similar a la sal de mesa (NaCl) la cual contiene cristales formados de iones positivos de sodio y negativos de cloruro. Mientras la sal de mesa (NaCl) no funde por debajo de los 800 ºC, la mayoría de los LIs se mantienen líquidos a temperatura ambiente. El punto de fusión del cloruro de sodio y cloruro de litio son 801 y 614 ºC, respectivamente. Debido a que estas sales fundidas convencionales exhiben un alto punto de fusión, su uso como solventes en diversas aplicaciones está severamente limitado. Sin embargo, Los líquidos iónicos a temperatura ambiente son líquidos generalmente hasta los 200 ºC.
Investigadores explican que los LIs permanecen líquidos a temperatura ambiente debido al hecho que sus iones no se empaquetan bien. La combinación de voluminosos y asimétrico cationes y aniones de forma uniforme (Figura 2) forman una estructura regular, es decir, una fase liquida. Los bajos puntos de fusión de los líquidos iónicos son el resultado de la composición química. La combinación de un catión orgánico más grande y asimétricos con una contraparte más pequeña e inorgánica resultara en una menor energía reticular y por eso el característico punto de fusión del medio iónico resultante. En algunos casos, incluso los aniones son relativamente grandes y juegan un rol en el descenso de los puntos de fusión.
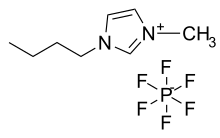
Figura 2. Ejemplo, catión asimétrico y anión simétrico [BMIM][PF6]
Propiedades de los Líquidos Iónicos.
Como solvente los LIs poseen grandes ventajas sobre los solventes orgánicos convencionales, lo cual los hacen compatible ambientalmente:
- Tienen la habilidad de disolver gran cantidad de materiales orgánicos, inorgánicos y organometalicos.
- Son altamente polar.
- Consiste en una débil coordinación de iones voluminosos.
- No se evaporan debido a su baja presión de vapor.
- Son térmicamente estables, aproximadamente hasta los 300 ºC.
- Poseen alta conductividad termal.
- Son alternativas polares no acuosas útiles para procesos de transferencia de fases.
- Las propiedades de los LIs como solventes pueden ser modificadas para una aplicación específica simplemente variando las combinaciones anión – catión.
Generalmente, las propiedades expuestas previamente son válidas para los líquidos iónicos comúnmente usados. Sin embargo, se debe tener en cuenta que hay muchos líquidos iónicos con aniones y cationes muy diferente entre ellos (Figura 3), por lo que en general las propiedades cubren un vasto rango. De manera que las propiedades expuestas antes no debe generalizarse para todos los líquidos iónicos existentes y los que puedan ser diseñados en el futuro.
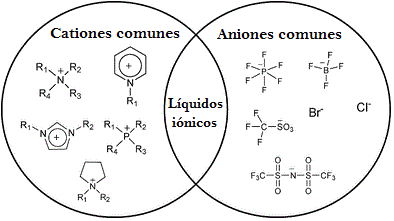
Figura 3. Ejemplo de algunos aniones y cationes empleados en líquidos iónicos
Aplicaciones de los líquidos iónicos.
Las propiedades químicas y físicas únicas de los líquidos iónicos permiten su aplicación en diversas áreas incluyendo como reactivo y medio de síntesis. Las diversas áreas donde los LIs pueden ser empleados comprenden: como solvente en síntesis orgánica, organometalica y catálisis; electrolito en electroquímica, en celdas de combustibles y solares; lubricante; fase estacionaria en cromatografía; matriz en espectrometría de masa; soporte para inmovilización de enzimas; en tecnología de separación; como cristal líquido; en síntesis de nano-materiales y como material para la preservación de tejidos; en la preparación de membranas catalíticas de polímero-gel; en la generación de materiales de alta conductividad; entre otras. En la actualidad las potenciales áreas de aplicación son numerosas y se incrementan rápidamente.
De todas estas aplicaciones he tenido la oportunidad de trabajar en una. La cual consiste en la síntesis de nano-materiales empleando líquidos iónicos como precursores. Estos nano-materiales son semiconductores con propiedades fotoluminiscente (Figura 4), que puede ser empleado ampliamente en el área de la optoelectrónica y como bio-marcadores. Espero más adelante hablar sobre este tema. Por otra parte, en otro trabajo de investigación el cual tuve el placer de ver cómo fue desarrollado, se logró observar la capacidad que poseen los liquido iónicos para la remover gases tóxicos como los es el sulfuro de hidrogeno (H2S) del petróleo. Esto demuestra la gran utilidad que le podemos dar a este tipo de sustancias químicas.

Figura 4. Material semiconductor fotoluminiscente obtenido a partir de líquido iónico
Futuro de los líquidos iónicos.
Como no todo lo que brilla es oro, el problema que presentan los líquidos iónicos en la actualidad es su rentabilidad. La producción de estos resulta muy costosa, en parte porque no son producidos en masa y además es necesario buscar otras vías para sintetizarlos donde se utilicen como precursores reactivos de menor costos. Por otra parte, la falta de información física, química y fisicoquímica de estas sustancias limitan su aplicabilidad. Estos problemas pueden ser resueltos siempre y cuando se apoye el uso de los líquidos iónicos en las diversas áreas ya expuestas. Esto significaría un gran paso en lo que consideramos como química verde.
Referencias.
- T. Welton, (1999). “Room temperature ionic liquids: Solvents for synthesis and catalysis.” Chem. Rev. 99, 2071–2084.
- Renner R., (2001). “Ionic liquids: an industrial cleanup solution.” Environ. Sci. Technol. 35, 410A–413A.
- Chiappe C. y Pieraccini D., (2005). "Ionic liquids: solvente properties and organic reactivity". J.of Phys. Org. Chem. 18, 275-297.
- Ionic liquid.
Being A SteemStem Member
Siempre odie la química -nunca le he conseguido el gusto ni nada parecido- pero no puedo negar que es la ciencia central. Con la que se comprende la vida y mediante ella se logran los mejores avances para la humanidad, en este momento puede no ser rentable los líquidos ionicos pero tiempo al tiempo.
Si es verdad, todo a su tiempo. Mientras más apoyen la aplicación de los líquidos iónicos existirá mayor interés por la industria en producirlos a gran escalas y optimizar la forma en que se obtienen, lo que esperemos se traduzca en compuestos químicos mas económicos.
Que interesante tema para profundizar, como tu dices quizás hoy no sea del todo rentable, Pero los líquidos iónicos podrían constituirse en una solución a futuro por todas las ventajas que ofrecen frente a los solventes convencionales.
Te pido permiso para compartir tu publicación en mi grupo de química en facebook y twitter.
Si este es un tema muy amplio e interesante, seguro te darás cuenta si busca mas información al respecto. Claro no hay problema esa la idea compartir el conocimiento, saludos.
Me apasiona este tema como químico. Voy a estar pendiente de tus próximas publicaciones. Saludos!